Thema: Risikomeldung/Rückruf
Artikel zum Thema
Chargenüberprüfung Tardyferon fehlen Charge und Verfall
Die Firma Pierre Fabre bittet um Überprüfung einer Charge Tardyferon Retardtabletten (Depot-Eisen(II)-sulfat). Mehr»
Rote-Hand-Brief Dinoproston: Risiko für Uterusruptur und Komplikationen
Die Zulassungsinhaber Pfizer und Ferring informieren mittels Rote-Hand-Brief über Maßnahmen zur Minimierung des Risikos für uterine Hyperstimulation,... Mehr»
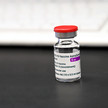
Rote-Hand-Brief Vaxzevria: Kontraindiziert bei früherem Kapillarlecksyndrom
Bereits in der vergangenen Woche hatte die Europäische Arzneimittelagentur (EMA) bekanntgegeben, dass das Corona-Vakzin Vaxzevria von AstraZeneca nicht bei... Mehr»
Die Firma Medicalfox ruft eine Charge Glukose-Fertigpulver zurück. Mehr»
MMR-Impfstoff Priorix ohne formale Freigabe
Der Dreifach-Impfstoff Priorix „axicorp“ geht aufgrund eines formalen Fehlers retour. Ein Patientenrisiko bestehe laut Hersteller nicht. Mehr»
FDA empfiehlt strenge Überwachung Ocaliva führt zu Leberschädigungen
Ocaliva ist zur Behandlung der primären biliären Cholangitis (PBC) auf dem Markt. Hierbei handelt es sich um eine seltene schwerwiegende Autoimmunerkrankung der... Mehr»
Rückruf Aluminium in Dronabinol Adrex
Die Firma Adrexpharma ruft mehrere Chargen ihrer Dronabinol-Kits zurück. Mehr»
Freiwillige Marktrücknahme Intrafusin enthält Partikel
Baxter informiert über Verunreinigungen in mehreren Chargen Intrafusin E Lösung. Hierbei handelt es sich um einen doppelten Rückruf. Die parenterale... Mehr»
Falscher Verdünnungsgrad Chargenüberprüfung bei Pflüger
Auf der Umverpackung der Nr. 2 Tropfen „Calcium phosphoricum D6“ von Pflüger ist ein Kennzeichnungsfehler. Anstatt der tatsächlich enthaltenen Potenzierung D6... Mehr»
Sevredol geht retour Morphin im Blister gebrochen
PB Pharma ruft vorsorglich mehrere Chargen des Medikamentes Sevredol zurück. Der Grund ist eine Meldung über gebrochene Tabletten im Blister. Mehr»
Medien zum Thema
- 1