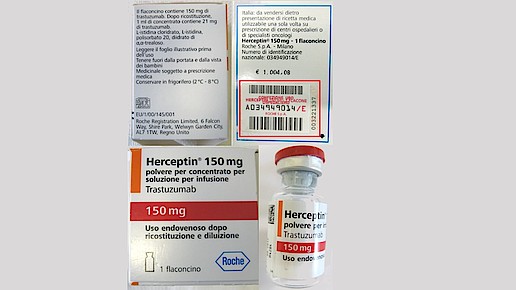
Illegal = gefälscht?
Im Fall der in Italien gestohlenen Medikamente Herceptin, Remicade,
Alimta und Humatrope herrscht eine gewisse Unübersichtlichkeit. Von
„illegaler“, „manipulierter“ oder „gefälschter“ Ware ist die Rede –
vorsorglich wurden vor Ostern alle potenziell betroffenen Chargen
zurückgerufen. Während die Behörden der Meinung sind, dass gestohlene
Medikamente grundsätzlich nicht verkehrsfähig sind, fühlen sich die
Reimporteure zu Unrecht an den Pranger gestellt.
Mehr als 30 Chargen haben die Europäische Arzneimittelagentur (EMA), das Paul-Ehrlich-Institut (PEI) und das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) bislang zurückgerufen. Während bei den anderen Präparaten bislang keine Manipulationen an der Ware entdeckt wurden, könnte es bei Herceptin zumindest in Einzelfällen ernste Risiken geben.
In einem aktuellen Rote-Hand-Brief warnt Roche vor Manipulationen an der Verschlusskappe und Einstichen im Gummistopfen. Außerdem sind demnach Fälle bekannt, in denen die Flasche anstatt des Pulvers eine Flüssigkeit enthielt. Eine chemische Analyse habe außerdem ergeben, dass zumindest in einem Fall kein Trastuzumab, sondern das Antibiotikum Ceftriaxon enthalten war.
Nach offiziellen Angaben ist die Ware aus Kliniken in Italien verschwunden, die selbst keine Großhandelserlaubnis hatten und damit zum Weiterverkauf nicht berechtigt waren. Aus internen Unterlagen von Roche geht aber hervor, dass Medikamente teilweise schon auf dem Transport gestohlen wurden oder verloren gegangen sind. In der Branche hält sich das Gerücht, dem Konzern seien im Dezember in Italien zwei ganze LKW-Ladungen abhanden gekommen.
Was mit den Infusionslösungen passiert ist und wohin sie weiterverkauft wurden, ist bislang allenfalls rudimentär bekannt. „Wir können bei gestohlener Ware nicht garantieren, dass die Transportkette eingehalten wurde“, sagt eine PEI-Sprecherin. Deshalb seien solche Medikamente illegal und damit per se nicht verkehrsfähig.
Aufmerksam gemacht wurden die Behörden durch einen britischen Zwischenhändler. Der hatte Herceptin-Flaschen in seinem Bestand entdeckt, bei denen die Chargennummern auf Flasche und Umkarton nicht identisch waren. Sein Lieferant, so stellte sich dann bei den Ermittlungen heraus, war nie von Roche beliefert worden und hatte auch andere Medikamente exportiert, bevor er Ende 2013 sein Geschäft einstellte.
Das britische Unternehmen wiederum hatte die Ware bereits nach Deutschland weiterverkauft. Außerdem wurden den Behörden zufolge im Lauf der Ermittlungen in Finnland, Österreich, Schweden und Großbritannien weitere „verdächtige“ Durchstechflaschen identifiziert.
In dem aus Deutschland bislang einzigen bekannten Fall war illegales Herceptin über zwei Großhändler in Großbritannien an den Parallelhändler gelangt. Aus Österreich ist bekannt, dass Haemato und Inopha betroffen sind. Herceptin-Reimporte gibt es hierzulande außerdem von Emra, Orifarm und Kohlpharma sowie von CC Pharma, Propharmed und Pharma Gerke, der Dermapharm-Tochter Cancernova und Cambridge Major Laboratories.
Unklar ist bislang, welchen Firmen gestohlene oder gar manipulierte Ware untergeschoben wurde. Angeblich sind mehrere Unternehmen betroffen, angeblich sind die drei großen Anbieter „sauber“. PEI und BfArM wollen das nun nachprüfen und haben von der EMA eine Liste mit allen deutschen Reimporteuren angefordert. Die Parallelhändler sollen detailliert Auskunft geben über alle Chargen der vier Produkte, die sie in den vergangenen zwei Jahren gehandelt haben – inklusive Lieferanten und Abnehmern.
Den Reimporteuren geht diese umfangreiche Abfrage zu weit, zumal die Rechtslage alles andere als eindeutig sei: Der Diebstahl sei zunächst ausschließlich Sache des Originalherstellers und allenfalls zivil- und straf-, aber nicht arzneimittelrechtlich relevant, heißt es. Wenn nur Einzelfälle als „manipuliert“ bezeichnet würden, könnten nicht gleich Dutzende Chargen aus dem Verkehr genommen werden.
Wenn aber, wie von den Behörden vertreten, schon die gestohlene Ware ohne irgendeine Manipulation als nicht verkehrsfähig zu betrachten sei, hätte es entsprechende Warnhinweise direkt nach dem Verschwinden geben müssen. Dass Roche seit Monaten nicht reagiert habe, zeige aber, dass wirtschaftliche Interessen im Spiel seien.
Ohnehin sei die angebliche Vertriebsbindung fraglich: Roche soll selbst eingeräumt haben, in Italien nicht nur Kliniken, sondern auch Apotheken und Großhändler beliefert zu haben. Entsprechende Hinweise stünden auch auf den Verpackungen.
„Hier werden gezielt mehrere Aspekte durcheinander gebracht, um eine gesamte Branche in Misskredit zu bringen“, kritisiert der Chefs eines Reimporteurs, der nach eigenem Bekunden nicht betroffen ist. „Warum werden Ross und Reiter nicht genannt“, fragt ein anderer Parallelhändler.