Thema: BfArM/EMA/FDA
Artikel zum Thema
Der Versorgungsmangel mit isotonischen Natriumchlorid-haltigen Lösungen ist beendet. Die Aufhebung wurde im Bundesanzeiger bekanntgegeben. Mehr»
Klimafreundlicher Inhalator Trixeo/Riltrava: Grünes Licht für neues Treibgas
Trixeo Aerosphere und Riltrava Aerosphere (AstraZeneca) sind in der EU die ersten inhalierbaren Arzneimittel, die in der neuen Zusammensetzung ein Treibgas mit... Mehr»
In Frankreich Evotec verkauft Standort an Sandoz
Der mitten in einem tiefgreifenden Umbau steckende Biotechkonzern Evotec will einen Standort in Toulouse an den Generikahersteller Sandoz verkaufen. Mehr»
In den USA bereits zugelassen PrEP: EMA empfiehlt Lenacapavir
Die Europäische Arzneimittel-Agentur (EMA) hat die Zulassung von Yeytuo (Lenacapavir, Gilead) zur HIV-Präexpositionsprophylaxe (PrEP) für Erwachsene und... Mehr»
Spontane Nebenwirkung Sumatriptan: Brustschmerzen bei Stillenden möglich
Triptane werden zur Akuttherapie der Migräne und des Cluster-Kopfschmerzes eingesetzt. Der Ausschuss für Risikobewertung im Bereich der Pharmakovigilanz (PRAC)... Mehr»
BfArM statt Sachverständigenausschuss OTC-Switches: Hersteller wollen neues Verfahren
Weil OTC-Switches immer wieder vom Sachverständigenausschuss für Verschreibungspflicht (SVA) abgelehnt werden, wollen sich die Hersteller für ein neues... Mehr»
Warnung vor gefährlichem Alkaloid Kratom: FDA geht gegen illegale Vermarktung vor
US-Arzneimittelbehörde FDA warnt derzeit vor illegalen, konzentrierten Produkten mit 7-Hydroxymitragynin (7-OH), einem starken opioidähnlichen Wirkstoff aus... Mehr»
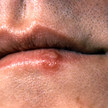
Sachverständigenausschuss Verschreibungspflicht Aciclovir-Bukkaltablette wird OTC
Zwei Wirkstoffe haben in dieser Woche vom Sachverständigenausschuss für Verschreibungspflicht eine Empfehlung für einen OTC-Switch erhalten: Aciclovir als... Mehr»
Kein Substitutionsausschluss BfArM: Bei Salbutamol auf Pulverinhalatoren austauschen
Salbutamol-haltige Dosieraerosole sind weiterhin von Lieferengpässen betroffen und Importe sichern die Versorgung. Zudem hat der Beirat für Liefer- und... Mehr»
Schwangerschaftsübelkeit Wegen Engpass: Cariban aus Spanien
Übelkeit gehört zu den ersten Anzeichen der Schwangerschaft und tritt meist ab der fünften Woche auf. Bringen konventionelle Therapien keine Besserung, kann die... Mehr»
Medien zum Thema
- 1
- 2