BfArM überwacht nur 90 Wirkstoffe
Lieferengpässe gehören zum Apothekenalltag. Pharmazeutisches Personal und Ärzte werden von den Defekten meist kalt erwischt, denn eine Meldepflicht gibt es nicht und nur wenige Wirkstoffe werden überwacht.
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) stuft Arzneistoffe in verschiedene Kategorien ein. Eine Gruppe sind die versorgungsrelevanten Wirkstoffe beziehungsweise jene, die mit einem akut erhöhten Versorgungsrisiko eingestuft werden. Die Behörde erarbeitet auf Basis der Empfehlung medizinischer Fachgesellschaften und der Weltgesundheitsorganisation (WHO) eine entsprechende Wirkstoffliste. Diese wird regelmäßig beim Jour Fixe angepasst.
Ob ein Arzneistoff versorgungsrelevant ist, hängt im Wesentlichen von zwei Faktoren ab. Die Grundlage bildet die Verschreibungspflicht. Außerdem muss der Wirkstoff für die Gesamtbevölkerung relevant sein und darf somit nicht als Orphan drug eingestuft sein. Die aktuelle Liste der versorgungsrelevanten Arzneistoffe beinhaltet mehrere Hundert Wirkstoffe und Wirkstoffkombinationen.
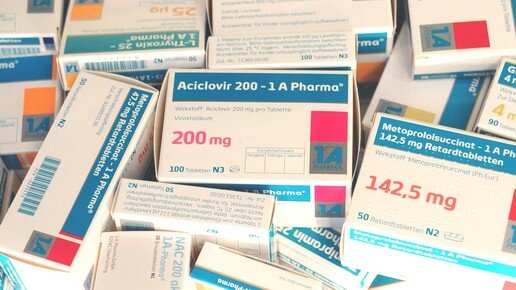
Gelistet sind unter anderem: Abacavir als Monopräparat und in Kombination mit Lamivudin, Acetylsalicylsäure zur intravenösen Anwendung, Aciclovir, Alendronsäure, Allopurinol, diverse Antibiotika wie Amoxicillin und Metronidazol. Gestrichen wurden Dimenhydrinat und Pankreatin. Versorgungsrelevant sind außerdem Insuline, Simvastatin, Maraviroc, Mometason, Pantoprazol, Permetrin, Steinkohlenteerlösung, Verpamil, Warfarin und Schmerzmittel wie Metamizol und Ibuprofen. Bei letzteren handelt es sich um Wirkstoffe, die in der Vergangenheit durch Lieferengpässe auffielen.
Beide Arzneistoffe unterliegen jedoch nicht der behördlichen Überwachung. Um vom BfArM überwacht zu werden, müssen Arzneistoffe zwar als versorgungsrelevant eingestuft sein, aber auch eines von drei weiteren Kriterien erfüllen. Es darf nur einen Zulassungsinhaber oder nur einen endfreigegebenen Hersteller oder nur einen Wirkstoffhersteller geben. Die Lister schrumpft auf 87 Wirkstoffe und Kombinationen zusammen.
Der behördlichen Überwachung unterliegen beispielsweise Acetylsalicylsäure i.v., Maraviroc, Permetrin, Trastuzumab, Tretinoin, Carmustin und Trastuzumab. Auch Propranolol ist zu finden, jedoch nur als Lösung zum Einnehmen und in der Indikation zur Anwendung bei Kindern.
Für Hersteller gibt es eine Selbstverpflichtung zur Meldung von Lieferengpässen. Diese gilt vor allem für Arzneistoffe, die in der Vergangenheit von einem Engpass betroffen waren. Ist ein Arzneimittel voraussichtlich länger als zwei Wochen im üblichen Umfang nicht lieferbar, oder kann eine deutlich erhöhte Nachfrage nicht bedient werden, spricht man von einem Lieferengpass. Hersteller werden gebeten, einen vorhersehbaren Engpass spätestens sechs Monate vor Eintreten zu melden. Eine Pflicht besteht jedoch nicht. Das BfArM hält die Meldungen in einer entsprechenden Liste fest.
























































APOTHEKE ADHOC Debatte